Atomaufbau
Wiederholung des Kern-Hülle-Modells Nach dem Bohr´schen Atommodell wird ein neues Atommodell nötig, um Phänomene erklären und beschreiben zu können, die mit dem Erlernten Modell nicht mehr erklärt werden können.
Einführung eines quantenmechanischen Atommodells. Aufgabe:
Lösen Sie das Arbeitsblatt Arbeitsblatt.
Download Periodensystem von Merck.
Klangfiguren als Resonazphänomen und Erklärungsversuch zu den Formen der Orbitale. Aufgabe: 2.4 Lewis und die Elektronenpaarbindung S. 54 Bindungsenthalpien
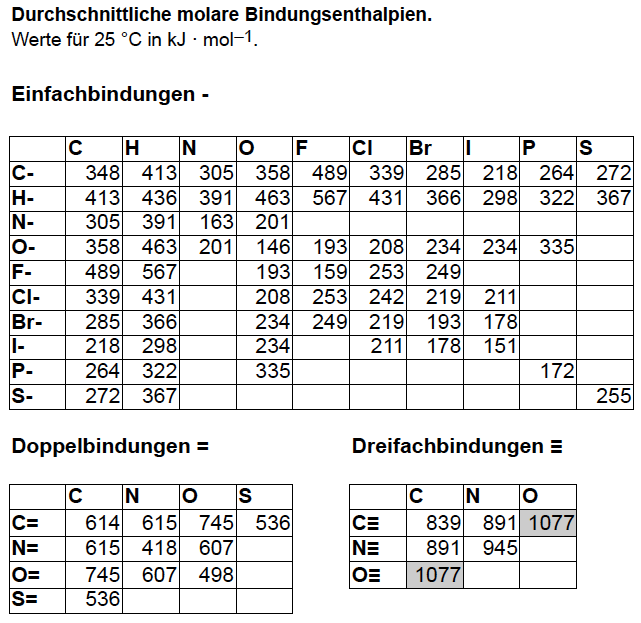
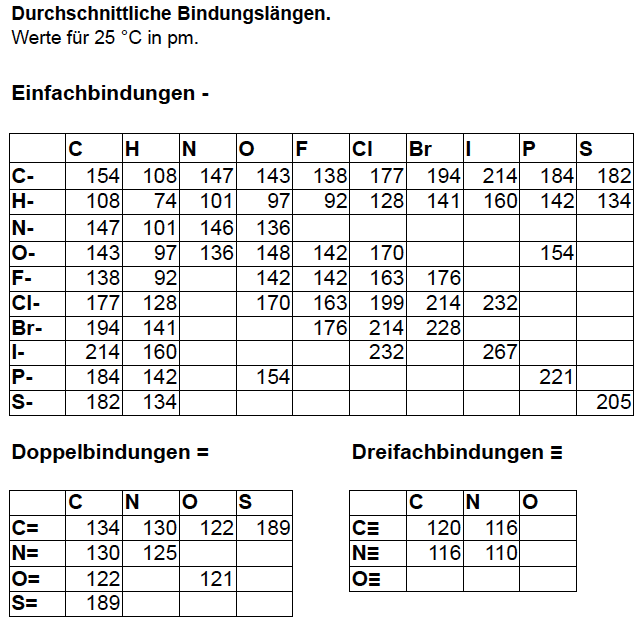
Berechnung von Bindungsenthalpien und Reaktionsenthalpien. Aufgabe: Berechne die Bindungsenthalpien der Reaktionen von Hex-2-in zu Cyclohexen zu Cyclohexan Bindungslängen
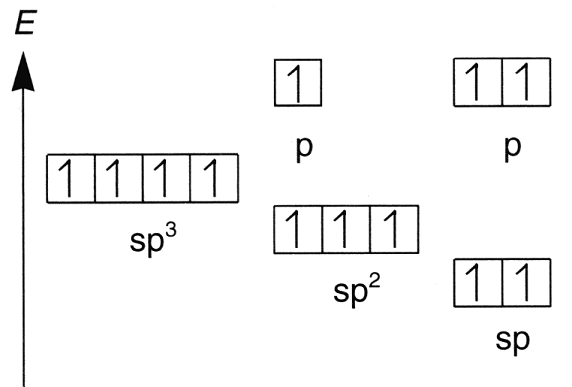
Einführung des Begriffes Mesomerie Mesomerie - die "Wahrheit" zwischen den Dingen S. 57 Hausaufgabe: 2.10 Hybridisierung - aus vier mach vier S. 68-69
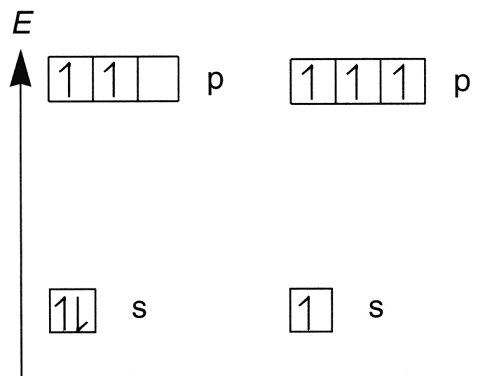
Grundzustand und angeregter Zustand eines Kohlenstoffatoms Hybridisierte Kohlenstoffatome
E-Mail an: chemiekoenig(at)gmail(dot)com
|